审阅:胡必杰、潘 珏
一、病史简介
男性,68岁,上海人,2017-8-28入住中山医院感染病科
主诉:间断发热近1月。
现病史:
2017-8-2患者无诱因出现发热,Tmax 39.8℃,伴乏力、恶心呕吐。8-10当地医院查WBC 14.49x10^9,N84.7%,hs-CRP 136.7mg/L;胸部CT未见明显异常,血培养为金黄色葡萄球菌(具体报阳瓶数及报阳时间不详),药敏试验显示,除了青霉素耐药外,对其余受试药物包括苯唑西林、环丙沙星、红霉素、复方新诺明、庆大霉素、克林霉素等均敏感。考虑甲氧西林敏感金黄色葡萄球菌(MSSA)引起的血流感染,予头孢他啶+青霉素+克林霉素(具体剂量不详)抗感染12天,体温高峰下降Tmax 37.8℃,但未至正常,8-22好转出院。
2017-8-24即出院后第2天,因再次出现高热Tmax 39.4℃,伴左腿麻木,无寒战,入住当地另一家医院。查WBC 16.35x10^9/L,N87.2%,hs-CRP 182.0mg/L,PCT 0.59pg/ml;8-25行胸腹CT报告“两下肺胸膜下少许间质增生;胆囊略炎变;双肾周围少许炎变,双肾小结石;腹膜后左侧腰大肌及左髂血管间隙囊状结构,神经源性/淋巴源性占位可能;肠道积粪较多”。头颅MRI无明显异常;予替考拉宁+左氧氟沙星抗感染2天仍高热。于2017-8-28为明确发热原因转入至上海中山医院感染病科。聽
既往史:外院住院期间发现有糖尿病,予甘舒霖降糖,血糖控制欠佳;高血压病史10年,予络活喜降压治疗。否认近期外伤、针刺伤、纹身、皮损等;5年前曾有腰椎摔伤史。
二、入院检查及诊疗(2017-8-28)
体格检查:
T38.4℃, P88 次/分, R20 次/分, BP166 / 85mmHg 。心肺检查正常。肾区无叩击痛。四肢肌力和感觉均正常。
实验室检查:
血常规:WBC:12.07,N:84.1%聽
炎症标志物:hsCRP: 120mg/L,ESR: 91mm/H,PCT: 聽0.04ng/ml,SF 1391ng/mL
糖化血红蛋白:8.0% 聽 聽 聽 聽 聽 聽 聽
肝肾功:ALT/AST 56/32U/L,Cr 74μmol/L
电解质:Na 127mmol/l,K 4.2mmol/l,Cl 90mmol/l
细胞免疫:CD4 683cells/ul,CD8 100cells/ul,CD4/CD8 6.8
肿瘤标记物:均阴性
自身抗体:(-)
T-SPOT A/B:0/0
血培养(4瓶同时于10h报阳):革兰阳性球菌。

辅助检查:
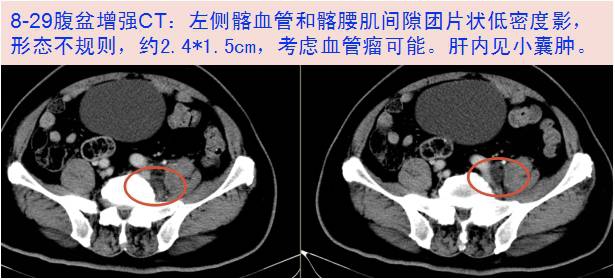
三、临床分析
患者老年男性,急性起病,发热近1月,无明显伴随症状,炎症志物明显升高,血培养为金黄色葡萄球菌(MSSA),来源不明。抗感染治疗起初有效,但很快又呈现发热,炎症标记物持续升高。再次发热后予以替考拉宁联合左氧氟沙星抗感染,效果不佳。据此,考虑诊断如下:
1、金葡菌隐匿部位感染合并血流感染,感染部位包括:
皮肤软组织感染:大多数为金葡菌感染引起,可有深部软组织感染、刺伤感染、压疮感染等复杂感染,也可有单纯性皮肤及软组织感染。患者有糖尿病史,血糖控制不佳,为该类细菌的易感人群,需详细问诊、查体和影像学检查,寻找可能的感染源线索。
骨及关节感染:金葡菌骨髓炎多继发于局部外伤或菌血症后,局部疼痛可为唯一症状或伴有低热。脊椎骨髓炎在胸腹部影像上,如轻症或早期,可能较难发现椎体病变,所以阴性结果尚不能排除该诊断。该患者有腰椎外伤史,但时间比较久远。
心内膜炎:金葡菌也是心内膜常见病原体,多急性病程,有寒战、高热及毒血症征象,并可伴有迁徙性病灶,如多发肺内病灶等。该患者心超未提示瓣膜赘生物,故本病可能小,必要时进行经食道的心脏超声以进一步排除。
2、金葡菌血流感染合并其他病原体引起的感染:
结核感染:最常见感染部位为肺,骨关节结核也较多见,多好发于脊椎,其次为膝、髋及肘关节等,发病缓慢,可伴有午后低热、夜间盗汗。病变处可形成不红、不热脓肿,即冷脓肿,活动时血沉增快,T-SPOT大多阳性,病变处脓液可找到抗酸杆菌,X线检查可见骨质疏松、骨质破坏、椎间隙狭窄或脓肿阴影。该患者有糖尿病史,CT提示腰椎旁低密度影,尚不能排除结核。
布鲁氏菌病:一种人畜共患病,多慢性起病,多数有牛羊接触史,急性期可表现为发热、乏力、多汗、肌肉及关节疼痛、肝脾淋巴结肿大,可通过抗体检测进一步明确。
3、金葡菌血流感染合并非感染疾病:该患者老年男性,发热3周以上,抗感染效果不佳,腹盆部CT增强提示左侧髂血管和髂腰肌间隙团片状低密度影,考虑发热待查,合并其他非感染性疾病如血液系统恶性肿瘤不能排除。
四、进一步检查、诊治过程和治疗反应
8-29 入院后抽取的血培养,10h 4瓶报阳,涂片为革兰阳性球菌,考虑金葡菌血流感染可能大,由于先前抗感染效果不佳,换用万古霉素1.0g q8h治疗。
8-30 出现解尿困难、尿潴留(500ml),考虑前列腺肥大尿道梗阻,予留置导尿;泌外科会诊加用哈乐对症。因仍高热,故再次血培养。
8-31 入院后抽取的血培养及药敏正式回报为MSSA,抗金葡菌治疗降级为头孢唑林2.0g q8h+阿米卡星0.6g qd抗感染。
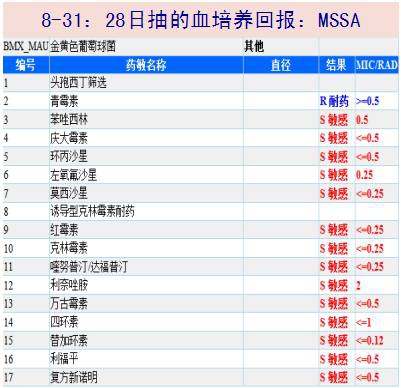
9-02 因持续高热不退,炎症标志物无明显下降,考虑混合感染可能,加用比阿培南0.6g q12h。
9-04 再次评估抗感染效果:患者体温高峰、炎症标志物下降不理想,8-30再次血培养仅1瓶报阳(且报阳时间达36h),单纯的金葡菌血流感染,不能完全解释持续发热原因。因此,改用米诺环素替换比阿培南以覆盖可能的特殊病原体。同时做骨髓穿刺、PET/CT,进一步寻找发热原因及隐匿病灶。
9-04 骨髓涂片+活检未见明确肿瘤依据,骨髓细菌培养阴性。
9-05 PET/CT提示第4/5腰椎结核伴左侧椎旁冷脓肿形成、相应水平椎管及腰4/5椎间盘累及可能,左侧髂血管旁淋巴结、骶孔神经累及不除外。
9-06 腰椎增强MRI提示:腰4、5信号改变伴椎旁软组织,考虑炎性病变,结核可能大。随停头孢唑林,试用“异烟肼+利福平+阿米卡星+利奈唑胺”抗结核并兼顾MSSA的治疗。
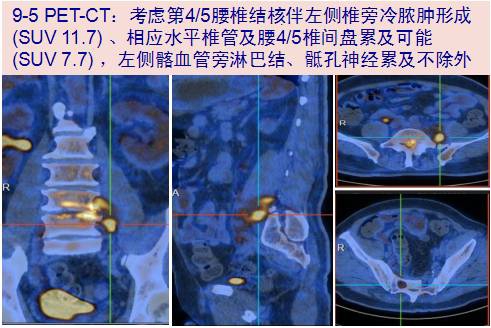
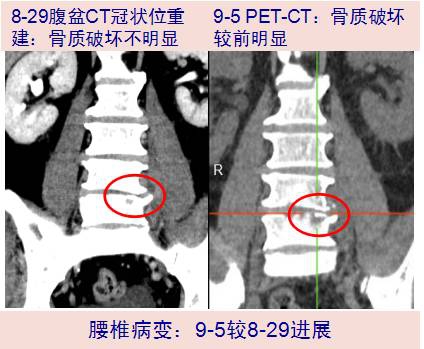
9-07 教授查房:PET-CT、腰椎MRI均提示结核不除外,但患者起病较急,外院胸部CT、我院PET-CT示双肺未见明显结核活动性病灶,入院T-spot A/B 0/0,结核支持证据不多。患者反复血培养提示金葡菌感染,金葡菌易可引起骨关节感染,床旁追问病史患者女儿诉发热前曾因左腿麻木外院行针灸治疗;综合考虑金葡菌至腰椎及软组织感染、血流感染可能大,结核感染不除外。嘱:①复查T-SPOT;②骨科会诊;③患者曾诉下腰痛,影像学反复提示左侧腰大肌及髂血管间隙病变性质不明,请放射科再次阅片;④介入超声会诊是否可行椎旁炎症部分穿刺及微生物培养明确病灶性质。
9-09 复查T-SPOT回报 A/B 2/0;骨科会诊考虑脊柱结核影像学表现不典型,化脓性感染可能大,可符合金葡菌感染;介入超声会诊因穿刺途径受限无法穿刺;放射科阅片比较入院时腹盆增强CT(8-29)中所示腰椎病灶及PET/CT(9-5)病灶,局部骨质破坏短时间内进展明显,结合病史,可符合MSSA腰椎及周围软组织感染合并血流感染可能大。
9-11 综合骨科、放射科等会诊意见,考虑活动性骨结核证据不足,停异烟肼、阿米卡星,因利福平对MSSA骨关节感染效果佳,暂保留。
间断夹闭导尿管锻炼膀胱功能后,9-12予拔除导尿管后患者仍诉解尿困难,随访残余尿250ml,考虑椎旁感染致骶孔神经累及引起神经源性膀胱可能大,再次留置导尿。
9-18 体温正常10天,复查炎症标志物CRP明显下降,血WBC正常,但ESR尚高。出院并带口服抗感染药物继续治疗。调整方案为利奈唑胺联合左氧氟沙星。仍留置导尿管,嘱患者泌外科随访完善尿动力学检查和评估拔除导管的时机。
出院后体温平,WBC、CRP正常,ESR维持在50mmol/L左右,9-29利奈唑胺减量0.3g q12h po,继续左氧氟沙星0.4g qd po,再次尝试拔除导尿管,诉解尿困难较前好转,但仍有解尿费力,复查残余尿50ml;10-27门诊复查腰椎MRI:与9-6基本相仿,继续随访中…
五、治疗后反应
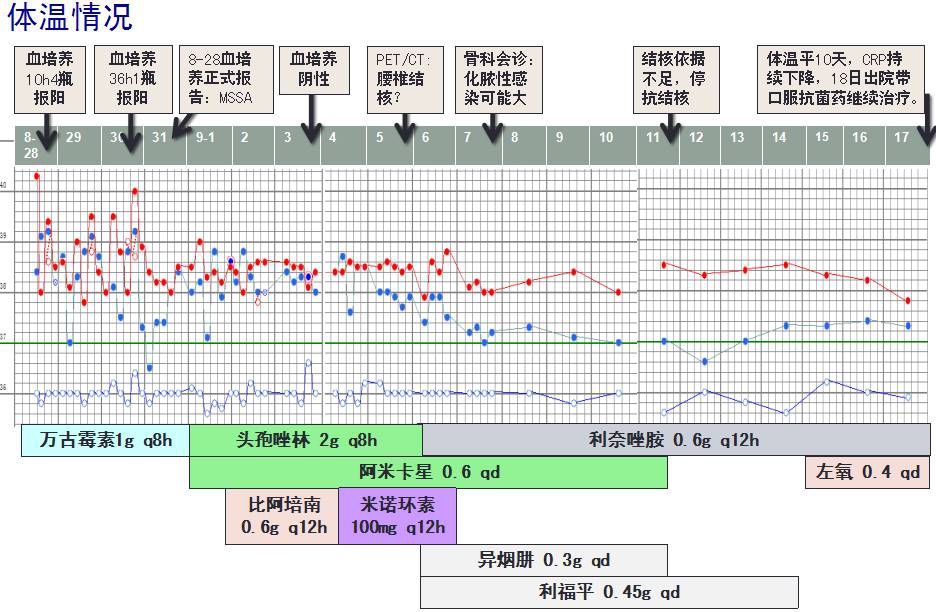
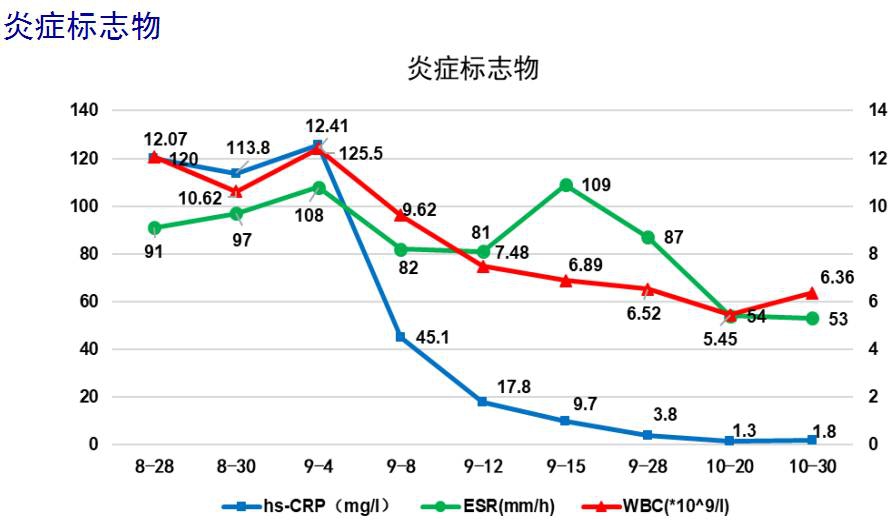
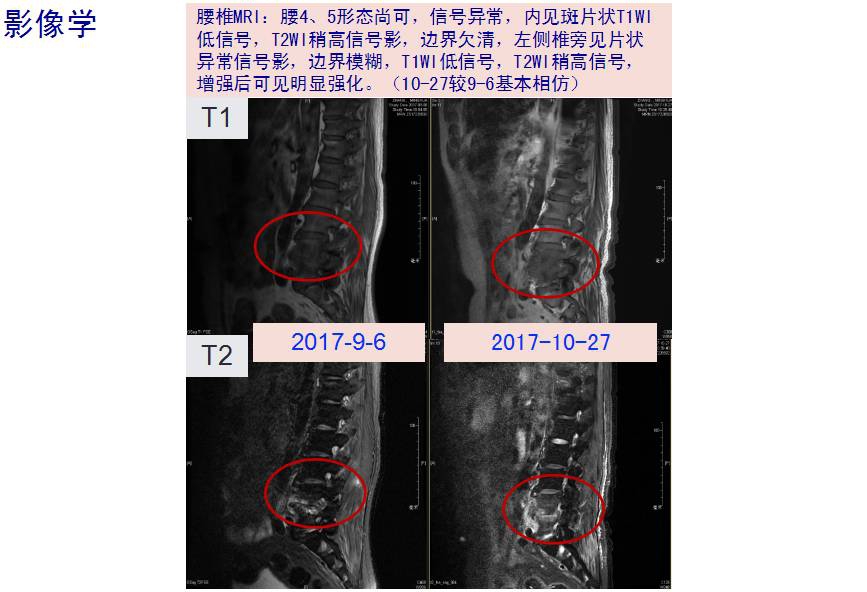
六、最后诊断与鉴别诊断
最后诊断:
1、金葡菌腰椎骨髓炎(伴菌血症)
2、神经源性膀胱(椎旁感染致骶孔神经累及可能)
诊断依据:
老年男性,急性病程,有糖尿病基础,发热近1月,曾行腰部针灸,炎症标志物明显升高,多次血培养提示MSSA,PET-CT及腰椎MRI增强提示第4-5腰椎及周围软组织炎症,抗金葡菌治疗有效,故诊断明确。
七、经验与体会
原发性脊柱骨髓炎在50-70岁患者中的发病率明显升高,可达6.5/10万,占骨髓炎中3-5%。腰背痛合并感染时需考虑该疾病,但症状无特异性,一般从出现症状到X片提示骨髓破坏需要3-6周的时间,常常延迟诊断,有研究统计其平均确诊时间为2-4月。而该病的延迟诊断可能会导致永久性脊髓损伤甚至瘫痪。MRI诊断脊柱感染的准确率达94%,PET-CT可协助发现慢性骨髓炎,而PET-CT阴性时可以排除骨髓炎的诊断[1]。
发热待查因其病因复杂、多样,至今仍是内科医生的噩梦。在寻找发热原因上需要拓宽思路,尤其是当有效抗感染基础上仍有发热时,需积极寻找潜在病灶及发热原因。该患者抗金葡菌治疗后血培养转阴,但仍有发热、炎症标志物下降不明显,需考虑是否有深部感染病灶所致。深部感染病灶通常隐匿、可无局部症状,常规影像学检查表现不特异,临床较易漏诊或延迟诊断。近年来发现PET-CT除在恶性肿瘤的筛查及评估方面存在优势,在部分感染性疾病中亦可以协助寻找隐匿感染灶,但PET-CT价格昂贵、辐射剂量较大,临床因综合评估后慎重选择该检查。
伴有菌血症的骨关节感染,血培养分离的细菌和体外药敏试验,对临床选择敏感的抗菌药物,具有良好的指导意义。然而,本例起初外院使用替考拉宁、我院万古霉素、头孢唑林+阿米卡星治疗不佳,可能与局部化脓病灶和骨组织中药物浓度不高有关。利奈唑胺作为新型抗阳性药物,在骨关节组织中浓度高、同时口服生物利用度高,虽然其为抑菌剂,血流感染不作为首选,但该患者在其他抗阳性菌治疗效果不佳情况下,选择以利奈唑胺为基础的联合方案,获得了非常好的疗效。有研究发现骨关节感染时利奈唑胺合并利福平,可明显减少血流感染发生,优于利奈唑胺单用[2]。脊柱骨髓炎有建议需要较长疗程,通常约为3个月,长期服用利奈唑胺,则需密切注意骨髓抑制、周围神经损害、视神经炎等不良反应。
参考文献
Berbari EF, et al. 2015 IDSA Clinical Practice Guidelines for the Diagnosis and Treatment of Native Vertebral Osteomyelitis in Adults. Clin Infect Dis. 2015 Sep 15;61(6): e26-46.
Dryden, MS. Linezolid pharmacokinetics and pharmacodynamics in clinical treatment. J Antimicrob Chemother, 2011. 66 Suppl 4: p. iv7-iv15.